Op 9 februari 2019 wordt de Europese Richtlijn Vervalste geneesmiddelen van kracht. Vanaf dan moeten de meeste voorschriftplichtige en terugbetaalbare geneesmiddelen die in de handel worden gebracht veiligheidskenmerken dragen. Bij elke schakel in de distributieketen worden deze veiligheidskenmerken gecontroleerd zodat de echtheid van het geneesmiddel bij aflevering kan worden gegarandeerd.
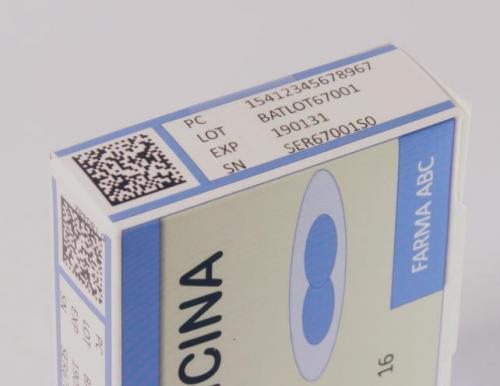
De veiligheidskenmerken bestaan uit een unieke, tweedimensionele matrixcode en een “anti-tampering device”, een middel tegen knoeien met de verpakking. De unieke matrixcode wordt door de geneesmiddelproducent via een beveiligd netwerk geactiveerd in een database. De groothandelaar controleert deze code en ook bij aflevering aan de patiënt in een apotheek of in het ziekenhuis wordt deze unieke code op de verpakking gescand en vergeleken met de code in het verificatiesysteem. Die controle maakt het mogelijk de patiënt en de farmaceutische sector tegen vervalste geneesmiddelen en namaak te beschermen. Het anti-tampering device of middel tegen knoeien is een verzegeling, label of doordruklijn zodat een verpakking niet ongemerkt kan worden geopend.

De Richtlijn Vervalste geneesmiddelen vereist dat het verificatiesysteem door de sector zelf moet ontwikkeld worden. In België heeft de farmaceutische sector hiervoor de vzw BeMVO (Belgian Medicines Verification Organisation) opgericht. De kost van de oprichting van het Belgische verificatiesysteem wordt zo gedragen door de geneesmiddelenindustrie in België en komt niet ten laste van de patiënt.
BeMVO heeft in overleg met het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG) een “alert”-procedure uitgewerkt bij “alerts” of foutmeldingen bij het scannen van een product. Deze stappenprocedure, de eerste van zijn soort in de Europese Unie, moet gevolgd worden in geval van foutmeldingen bij het scannen van producten. De ervaring bij het ontwikkelen en testen van het systeem heeft aangetoond dat vooral in de eerste weken na het operationeel worden van het systeem er nog heel wat foutmeldingen kunnen worden verwacht waarbij het niet om namaak zal gaan. Het FAGG heeft daarom enkele praktische richtlijnen voor het behandelen van problemen in de opstartfase gebundeld in een omzendbrief. Geneesmiddelen die voor 9 februari 2019 in de handel werden gebracht en waar de code nog niet op de verpakking staat mogen vanzelfsprekend nog worden afgeleverd aan de patiënt.
Bekijk de video voor meer uitleg
Meer informatie
BeMVO (Belgian Medicines Verification Organisation)
Richtlijn Vervalste geneesmiddelen (Richtlijn 2011/62/EU of Falsified Medicines Directive, FMD)
Praktische aanbevelingen bij het nieuwe verificatiesysteem tegen vervalste geneesmiddelen

